ДЕКОРАТИВНАЯ ОБРАБОТКА ЮВЕЛИРНЫХ УКРАШЕНИЙ
Декоративная обработка ювелирных украшений может осуществляться механическим способом (чеканкой, гравировкой) и нанесением защитно-декоративных покрытий (эмалированием, чернением, оксидированием, золочением, серебрением, родированием).
Цель декоративной обработки ювелирных изделий - облагородить их, придать им яркость и новые внешние качества. Выполняется декоративная обработка как вручную, так и с применением специального оборудования (в условиях промышленного производства).
ГАЛЬВАНИЧЕСКИЕ ПОКРЫТИЯ
Процесс гальванического покрытия представляет собой осаждение одного металла на другой в среде электролита. В ювелирной промышленности в качестве гальванических покрытий используют золото, серебро, реже родий и сплавы золота. Цель таких покрытий — придать изделиям определенный декоративный вид, повысить их механическую характеристику.
Процессы золочения и серебрения известны давно, родирование стало применяться в последние годы, в основном для покрытий изделий из белого золота и платины. Покрытия из сплавов, особенно из сплавов золота, с введением в них никеля, кобальта, меди, серебра позволили расширить ассортимент ювелирных изделий, улучшить их внешний вид, повысить срок службы, а главное — сократить расход драгоценных металлов.
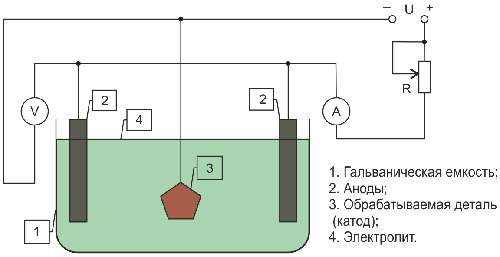 Покрытия, полученные в процессе гальванизации, отличаются высокой прочностью, а сам процесс — экономичностью. В качестве электролитов при гальванизации используются растворы солей и кислот. Сущность электролитического осаждения состоит в следующем. При пропускании постоянного тока через электролит, куда уже помещены покрываемые изделия и металл покрытия, начинается химическая реакция: к катоду (покрываемые изделия) как отрицательному электроду устремляются положительные ионы металла покрытия, а к аноду (металл покрытия) как положительному электроду — отрицательные ионы кислотных водных остатков.
Основным оборудованием для проведения процессов гальванических покрытий являются ванны для химического и электрохимического обезжиривания изделий и для нанесения гальванических покрытий.
Ванны для обезжиривания изготовляют в виде сварной прямоугольной ёмкости из 3—5 миллиметровой листовой стали. Объем ванн колеблется от 100 до 200 л. Ванны для обезжиривания снабжаются системой подогрева и бортовыми вентиляционными устройствами. Для удаления с поверхности раствора пены и масла ванны имеют специальные устройства в виде карманов.
 Ванны для нанесения гальванических покрытий выполняют, как правило, из коррозионно-стойкой стали с покрытием изнутри эмалью или изоляционными материалами — винипластом, тефлоном. Ванны, выложенные изнутри винипластом или тефлоном, применяют в процессах гальванизации при использовании кислых электролитов, Имеются также стеклянные ванны, которые предназначены для родирования, как обеспечивающие особую чистоту электролиза. По форме ванны делят на сварные прямоугольные (стационарные) и барабанные или колокольные (вращающиеся). В барабанных или колокольных ваннах производят золочение мелких изделий, причем скорость золочения в них на 20—30% ниже, чем в стационарных. Вместимость ванн различная: 15—50 л — для золочения, 100—500 л— для серебрения, 1—2 л — для родирования. Нагрев электролита в ваннах производится двумя способами: действием пара (горячей воды) или электрического тока. Электролит в ванне перемешивается либо давлением сжатого воздуха, либо вращением катодной штанги.
 Подготовка ювелирных изделий к гальваническому покрытию. Перед нанесением гальванических покрытий на изделия проводится тщательная подготовка их поверхности. Различают два вида подготовки: механическую и химическую. Механическая подготовка — полирование, крарцевание — позволяет исправить, устранить дефекты, придать изделиям блестящий зеркальный вид. Химическая подготовка предусматривает удаление с изделий жирных загрязнений и оксидов и называется обезжириванием. Обезжиривание проводится в два этапа: сначала в органических растворах, а затем в щелочных. Обезжиривание в щелочных растворах подразделяют на химическое и электрохимическое.
Обезжиривание изделий в органических растворах
Химическому обезжириванию подвергаются не все изделия, а лишь определенная их группа
Составы электролитов, режим работы ванн при электрохимическом обезжиривании
Очистка изделий при электрохимическом обезжиривании происходит в процессе электролиза — пропускания постоянного тока через электролит, когда сами изделия играют роль катода. Применяемые при этом электролиты неоднородны по составу компонентов, так как одни из них используются для очистки изделий, предназначенных для золочения, другие — для очистки изделий под серебрение, третьи — для очистки изделий под родирование.
Растворы для химического обезжиривания
изделий в процессах золочения, серебрения, родирования
После окончания химического или электрохимического обезжиривания изделия промывают последовательно в горячей (50—70 °С) и холодной проточной воде. Завершающей операцией подготовки поверхности изделий перед проведением процесса осаждения металла является декапирование их — очень слабое протравливание (шерохование) верхнего слоя в целях более прочного сцепления покрытий с основой. Декапирование изделий под золочение производится в 5—7 %-ном растворе соляной кислоты, изделий под серебрение — в 5—10 %-ном растворе серной кислоты, изделий под родирование — в 5 %-ном растворе серной кислоты. Время выдержки и температура растворов составляют соответственно 10—30 °С и 18—25 °С.
 Золочение. В ювелирной промышленности золочение является одним из основных процессов гальванических покрытий. Золочению, как правило, подвергают ювелирные украшения из недрагоценных металлов, но золотят также изделия из серебра и золота при реставрации и обновлении. Золочение бывает матовое и блестящее. Матовое золочение — широко известный традиционный вид золочения.
Блестящее золочение — сравнительно молодой прием гальванического покрытия. Преимущества этого вида золочения состоят в том, что он позволяет сократить потери золота и механизировать сам процесс. Золочение блестящее обеспечивается введением в состав электролита блескообразующих добавок и изменением режима электролиза.
Матовое золочение. В электролиты для матового золочения входят (г/л): цианистый калий KCN — 10—90, металлическое золото Аu — 0,5—15 (либо золото в виде дицианоаурата — 4—10), кислый фосфат калия — 50—100 (либо без него). Электролиз идет при температуре 55—70 °С и плотности тока 11—12 А/дм2. Время выдержки определяется исполнителем визуально до получения качественного покрытия. Электролиз с применением элетролита без кислого фосфата калия и с золотом в виде дицианоаурата проходит при температуре 45—55 °С и плотности тока 0,2—0,5 А/дм2.
 Блестящее золочение. В состав электролита для блестящего золочения входят следующие компоненты (г/л): цианистый калий — 15, металлическое золото — 2, олеат натрия — 0,2, поташ — 1—100. Электролиз идет в течение 5—10 мин при температуре элетролита — 60 °С и плотности тока 0,5—0,6 А/дм2. При золочении золотых изделий (реставрации) применяют электролиты с повышенным содержанием цианистого калия, например электролит (г/л): цианистый калий — 20—22, дицианоауратный калий — 3—4. Температура элетролиза равна 65—70 °С, а плотность тока составляет 0,13—0,2 А/дм2.
В последние годы при проведении процессов гальванических покрытий широкое распространение получили кислые нецианистые (нетоксичные) электролиты, обеспечивающие осаждение блестящих покрытий сплавами золото — никель и золото — кобальт.
Составы электролитов для золочения сплавами
золото – никель и золото – кобальт, режимы работы ванн
Технологический процесс золочения ювелирных украшений в кислых нецианистых электролитах выполняется в следующей последовательности: обезжиривание в органическом растворе, просушивание, загрузка (монтаж) изделий на приспособление, обезжиривание электрохимическое, промывка (последовательно) в горячей и холодной воде, просушивание, снятие (демонтаж) изделий с приспособления, взвешивание (100%-ное), загрузка на приспособление, декапирование, промывка (последовательно), в проточной и дистилированной холодной воде, золочение, первое, второе и третье улавливание, промывка в холодной воде, промывка в горячей воде, просушивание, снятие изделий с приспособления, взвешивание (100%-ное, за исключением пустотелых изделий), галтование, промывка (последняя) в холодной и горячей воде, просушивание, контроль. Сушка изделий осуществляется в сушильных шкафах при температуре 70—100°С.
 Последовательность выполнения операций должна соблюдаться неукоснительно — в этом залог безотказной и длительной работы ванны для золочения. Необходимо также постоянно контролировать и корректировать состав электролитов золочения: определение количества золота приводится ежедневно, кобальта или никеля — один раз в три-четыре дня. Нельзя допускать ни снижения, ни завышения концентрации кобальта, никеля, золота — это автоматически приводит к браку в изделиях.
Нередко применяются составы электролитов золочения, позволяющие получать покрытия красного (золото — медь) и зеленого (золото — кадмий) оттенков. Характерная особенность этих электролитов — высокая производительность (10—12 мкм/г).
Составы электролитов для золочения сплавами золото –
медь и золото – кадмий, режимы работы ванн
Контроль позолоченных изделий. Все позолоченные изделия контролируются по внешнему виду, толщине покрытия, содержанию золота в них. Внешний вид проверяется визуально, толщина покрытия — весовым методом, т. е. все изделия, взвешиваются до и после золочения. Результаты взвешивания сопоставляются с нормами наложения золота на каждый вид изделий. Обычно норма толщины золотого покрытия ювелирных украшений составляет 0,5—1 мкм. Исключение составляют обручальные кольца из серебра — толщина их золотого покрытия равняется 10 мкм.
Контроль за содержанием золота в покрытиях основан на золочении контрольных пластинок одновременно с партией изделий, последующим переведением покрытия с пластинки в раствор и количественного определения золота и легирующего металла.
Пример несложного приема золочения ювелирных украшений. Для золочения протиранием 1 г хлорида золота растворить в 10 г воды, добавить чуточку (на кончике ножа) селитры, тщательно перемешать. Затем вылить раствор на заранее приготовленные льняные лоскутки (тряпочки), а после того, как лоскутки просохнут, их необходимо сжечь. Образовавшуюся окалину растереть в порошок и перемешать с подсоленой водой. Полученным раствором (с помощью пальца) протереть места, которые необходимо позолотить (предварительно отполированные). Если нужно получить красный цвет, то в раствор добавляют медь, если бледно-желтый — серебро.
 Удаление позолоты. Снятие золотого покрытия с. ювелирных украшений при необходимости осуществляется гальваническим путем — процесс, обратный золочению. Изделия являются анодом (положительный электролит), а снимаемая с них позолота — катодом (отрицательный электролит). Процесс снятия позолоты идет в электролите в течение 3—5 мин при большой силе тока. Широко применяются электролиты следующих составов: 1 л воды, 85 г цианистого калия, 192 г фосфорнокислого бикарбоната натрия или 1 л воды, 30 г желтой кровяной соли, 30 г поташа, 30 г поваренной соли, или 2,5—3 л воды, 200 г цианистого калия, 100 г кровяной соли, 75 г соды.
 Серебрение. Многие ювелирные украшения изготовленные из недрагоценных металлов (латуни, мельхиора, нейзильбера) в целях улучшения их декоративного вида подвергают серебрению. Процесс серебрения осуществляется, как правило, в электролитах, содержащих свободный цианистый калий. Чтобы обеспечить прочное сцепление между металлом изделий и серебряным покрытием и избежать контактного выделения серебра при погружении изделий в рабочую ванну, серебрение начинают либо с амальгамирования, либо с предварительного серебрения.
Амальгамированию подлежат изделия из сплавов на медной основе и содержащих значительные количества никеля. Амальгамируют изделия в течение 3—5 сек при температуре 15—25 °С в растворах следующего состава (в г/л): хлористая ртуть — 7,5 и хлористый аммоний — 4 или хлористая ртуть , 6—8, или ртуть азотнокислая — 8—10 и кислота азотная — 1—2, или цианистый калий — 60—70.
Изделия посудной группы вместо амальгамирования проходят этап предварительного серебрения в электролитах. Электролиз ведется в течение от 30 с до 4 мин при температуре 20—30 °С и плотности тока 1—2 А/дм2 в электролитах, состоящих либо из 1,5—4 г/л цианистого серебра и 90 г/л цианистого калия, либо из 2—3 г/л цианистого серебра и 45—50 г/л цианистого калия, либо из 3—5 г/л анодного серебра и 70—90 г/л цианистого калия, либо из 1—3 г/л азотнокислого серебра, 70—90 г/л цианистого калия и 20—30 г/л углекислого калия.
По завершению амальгамирования или предварительного серебрения изделия загружают (переносят) в ванну с электролитом основного серебрения. В практике ювелирного дела существует не один состав цианистых электролитов.
Составы цианистых электролитов серебрения и режимы работы ванн
Серебряные покрытия обычно получаются матовыми. Чтобы иметь блестящее серебряное покрытие, в электролит вводят блескообразующие добавки — серосодержащие вещества: тиосульфат натрия, сероуглерод и другие, содержание которых в электролите надо постоянно контролировать.
Применяют также электролиты, не содержащие свободного цианистого калия: железистосинеродистые, роданистосинеродистые и трилонатно-аммониевые. Недостатком железистосинеродистого электролита является необходимость применения нерастворимых анодов, когда электроосаждение серебра происходит только из элекролита. Роданистосинеродистый электролит позволяет использовать серебряные аноды и может работать без корректировки в течение месяца. Приемы бесцианистого серебрения позволяют отказаться от амальгамирования или предварительного серебрения изделий. Составы некоторых нецианистых электролитов серебрения и режимы работы ванн приведены в таблице.
Составы бесцианистых электролитов серебрения,
режим работы ванн
После окончания серебрения изделия извлекают из ванн, в течение 15—20 с промывают — сначала в ванне с улавливателем, а затем в проточной воде. Для уплотнения серебряного слоя изделия подвергают крацеванию, снова промывают последовательно в холодной и горячей воде (70—90 °С), после чего просушивают в сушильных шкафах (70—100 °С) и проводят контроль качества покрытия.
Контроль посеребренных изделий. Контроль серебряных покрытий производят по следующим и наиболее важным показателям: состоянию поверхности и толщине слоя. Состояние поверхности серебряных покрытий, как и золотых, определяется визуально: не допускается неравномерность оттенков и блеска, не должно быть пятен, подтеков, непокрытых мест, слой серебра должен плотно прилегать к основному металлу.
Толщина покрытия, как правило, определяется взвешиванием (100%-ным) изделий до и после серебрения. При химическом методе определения толщины серебряного покрытия необходимо слой покрытия перевести в жидкое состояние, т. е. растворить. Это достигается помещением изделия в емкость (фарфоровую чашку) со слабо подогретой смесью концентрированных кислот.
Определение местной (в заданной точке) толщины покрытия производится капельным методом. На поверхность покрытия пипеткой наносят каплю травящего раствора — азотной кислоты (1:1), выдерживают 30 с, затем фильтровальной бумагой или ваткой убирают каплю и наносят вторую, третью и т. д. до тех пор, пока не обнажится основной металл или подслой.
Пример несложного приема серебрения ювелирных украшений. Для серебрения протиранием 52 г нитрата серебра растворить в 100 г воды, добавить поваренную соль и тщательно размешать. Образовавшееся хлористое серебро отфильтровать, затем смешать с 10 г порошка винного камня и 15 г поваренной соли до получения густой кашеобразной массы. Указанной массой с помощью пальца протирать предназначенные для серебрения места до тех пор, пока не появится чистый серебряный цвет.
Удаление серебряного покрытия. Хорошо обезжиренные изделия на несколько часов помещают в охлажденную смесь 1 л водного раствора серной кислоты и 13 г азотной кислоты. Окончание процесса — удаление серебряного покрытия — контролируют визуально. Наблюдают появление пурпурного цвета, который быстро переходит в зелёный, после этого изделия необходимо промыть в воде, просушить, а оставшуюся на изделиях тонкую пленку снять мягкой щеткой. При этом откроется ровная, блестящая поверхность основного металла.
Родирование. Родиевые покрытия улучшают внешний вид изделий, химические и механические свойства металлов. Электролитические покрытия родием применяют для украшений из меди, латуни, мельхиора, никеля, сплавов серебра, золота, платины, палладия. Особенно же широкое распространение получило роди-рование украшений из белого золота и платины.
Технология нанесения родия довольно проста, но требует особо тщательного выполнения операций по подготовке поверхности изделий, подлежащих родированию. Для обеспечения зеркальности покрытий изделия должны быть хорошо отполированы и иметь параметр шероховатости поверхности не ниже 9-10-го квалитетов.
Процесс подготовки к родированию украшений из золота и платины ведется в такой последовательности: обезжиривание в органических растворителях, химическое обезжиривание, промывка соответственно в дистиллированной и проточной воде. Подготовка украшений из серебра и недрагоценных металлов требует несколько иного порядка: обезжиривание органическое, промывка в проточной воде, обезжиривание электролитическое, промывка в горячей (50–60 °С) воде, химическая обработка, промывка в проточной воде, декапирование.
Для проведения процесса родирования используют сернокислые и фосфорнокислые электролиты с большим содержанием кислоты, обладающие высокой рассеивающей способностью и позволяющие получать ровные блестящие покрытия. При этом в качестве анода применяют нерастворимые платиновые или родиевые пластины.
Достоинством сернокислых электролитов является их меньшая, чем у фосфорнокислых, чувствительность к загрязнениям. В состав сернокислых электролитов обычно входят (г/л): серная кислота — 45-90 и родий сернокислый — 2-4. Электролиз идет в течение 4-6 мин при температуре от 30 до 40 °С и плотности тока от 0,8 до 1,5 А/дм2. Применяются сернокислые электролиты и других составов, например 4-10 г/л родия сернокислого, 100-180 г/л кислоты серной, 5-10 г/л кислоты сульфаминовой. Время электролиза 2-10 мин, рабочая температура 15-20 °С, плотность тока 0,4-1,0 А/дм2.
Фосфорнокислые электролиты родирования применяются значительно реже. Состав их обычно таков (г/л): ортофосфорная кислота — 50, металлический родий — 2. Время электролиза 4-6 мин, рабочая температура от 20 до 60 °С, плотность тока от 0,3 до 5 А/дм2. По окончании родирования изделия проходят следующий цикл обработки: промывку с улавливанием в дистиллированной и горячей воде, промывку в этиловом спирте, просушивание в сушильных шкафах при температуре 80-90 °С. Контроль родиевых покрытий осуществляется визуально и 100%-ным взвешиванием изделий до и после родирования.
| 





